Des Progrès Spectaculaires
Grâce aux immenses succès récents en immunothérapie, certains patients atteints d’un cancer associé à un nombre élevé de mutations (jusqu’à plusieurs milliers) peuvent désormais espérer gagner plusieurs années de vie, voire bénéficier d’une cure durable, alors qu’ils auraient été condamnés il y a 2 ou 3 ans à peine.
Cependant, la majorité des patients ne peut pas bénéficier de cette avancée médicale majeure car le taux de mutations de leurs cellules tumorales est insuffisant pour permettre une activation de leur système immunitaire, nécessaire au rejet de leur(s) tumeur(s).
Cancer : Quelques chiffres
Le cancer, seconde cause de décès dans le monde, a tué environ 9 millions de personnes l'année dernière. Les experts estiment que ce chiffre aura augmenté de 70% en 2035. Globalement, le coût du cancer est quant-à-lui estimé à 1.2 trillion de dollars. En France, le cancer est la première cause de décès, totalisant environ un quart des décès chez les femmes et un tiers chez les hommes. Il est estimé qu’un Français sur deux sera confronté à un cancer au cours de son existence.
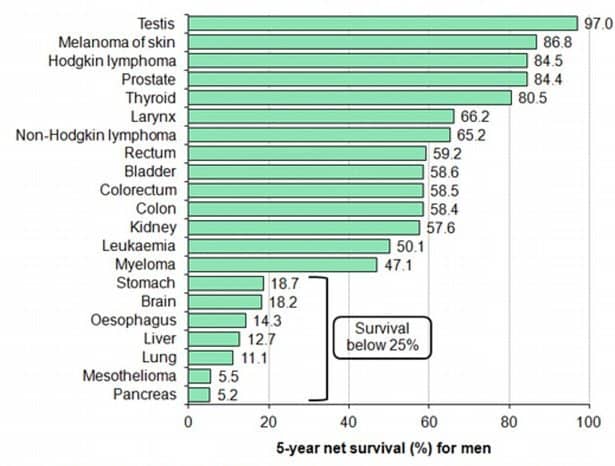
Au niveau mondial, les cancers les plus meurtriers chaque année sont ceux du poumon (1.7 millions de décès l'année dernière), du foie (788K), colorectal (774K), de l'estomac (754K) et du sein (571K).
Immunothérapie et checkpoint inhibitors
Contrecarrer les mécanismes d'évasion immunitaire
L’un des traits caractéristiques de tout cancer est sa capacité à progressivement échapper à la surveillance du système immunitaire, au travers de nombreux mécanismes complexes d’évasion immunitaire. Les approches modernes d’immunothérapie peuvent s’avérer particulièrement efficaces pour traiter les patients dont le système immunitaire a été activé initialement suite à la détection de cellules cancéreuses, puis est devenu anergique en raison d’un mécanisme de résistance immunitaire de la tumeur.
Les approches immunothérapeutiques de type checkpoint inhibitors permettent alors de restaurer la capacité d’action du système immunitaire face aux cellules cancéreuses, avec une efficacité qui augmente chaque année. Les anticorps thérapeutiques anti-CTLA4 (ipilimumab), anti-PD1 (nivolumab, pembrolizumab) et anti-PDL1 (atezolizumab) sont des checkpoint inhibitors désormais utilisés en routine et qui ont prouvé leur efficacité.
Seuls certains patients sont concernés
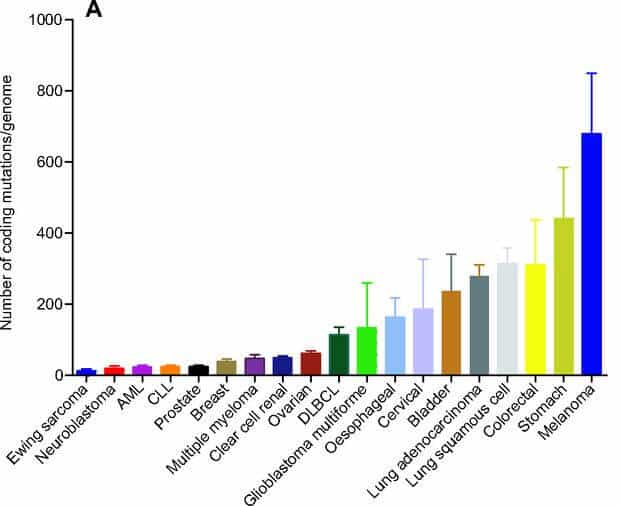
Près de 70% des cancers n’induisent pas (ou très peu) d’activation spontanée du système immunitaire en raison d’un trop faible nombre de mutations exprimées par les cellules cancéreuses. Ces cellules peu mutées sont en effet trop semblables à des cellules saines pour être reconnues par le système immunitaire.
Les approches d'immunothérapie telles que les checkpoint inhibitors n’étant alors pas indiquées pour ces patients, il est pertinent d’opter pour une thérapie qui activera le système immunitaire en redirigeant les cellules immunitaires vers le site de la tumeur.
Les thérapies ciblées

Cibler les cellules aberrantes
Les thérapies ciblées par anticorps ont un immense potentiel pour aider le système immunitaire à reconnaître et détruire des cellules cancéreuses.
A l’heure actuelle, ces anticorps anti-cancer sur le marché ou en cours de développement clinique sont conçus pour fixer une cible cancéreuse présente chez un maximum de patients. Ces cibles sont généralement des protéines naturelles surexprimées ou modifiées suite à une mutation dans le génome tumoral.
Quelles sont les mutations actionnables ?
Une limite majeure aux thérapies ciblées actuelles est que la vaste majorité des mutations présentes dans une tumeur sont non-actionnables, soit parce qu’elles sont patient-spécifiques, soit parce qu’il n’existe encore aucune thérapie les ciblant.
En conséquence chez les nombreux patients atteints d’un cancer peu muté, les cancérologues parviennent rarement à identifier une mutation actionnable. En outre, lorsqu'un patient présente une mutation actionnable, cette dernière est souvent trop peu représentée dans la tumeur pour permettre un traitement efficace.
Dans ces circonstances, la meilleure approche est de développer des traitements plus personnalisés en mesure de cibler spécifiquement les mutations ayant un réel intérêt clinique pour chaque patient.

